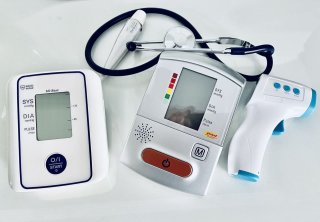
Государства Евразийского экономического союза подписали Протокол о внесении изменения в Соглашение о единых принципах и правилах обращения медицинских изделий (изделий медицинского назначения и медицинской техники) в рамках ЕАЭС.
Все материалы
Советом ЕЭК одобрено решение, которым внесены дополнения в Правила проведения исследований биоэквивалентности лекарственных средств, устанавливающие единые нормы подтверждения эквивалентности воспроизведенных (генерических) и гибридных препаратов для местного применения. Об этом в ходе брифинга, проведенного по итогам заседания Совета ЕЭК 15 февраля 2023 года, сообщила официальный представитель Евразийской экономической комиссии Ия Малкина.
Как сообщается на официальном сайте Коллегии ЕЭК, оценка является частью процедуры рассмотрения поступившего в Евразийскую экономическую комиссию заявления о возможных признаках недобросовестной конкуренции на товарном рынке лечебного питания.
Как сообщается на официальном сайте Коллегии ЕЭК, оценка является частью процедуры рассмотрения поступившего в Евразийскую экономическую комиссию заявления о возможных признаках недобросовестной конкуренции на товарном рынке лечебного питания.
Коллегия Евразийской экономической комиссии приняла Руководство по составлению документации по химическому и фармацевтическому качеству для лекарственных средств, применяемых в клинических исследованиях. Об этом сообщает пресс-служба Коллегии ЕЭК.
Департаментом технического регулирования и аккредитации Коллегии ЕЭК разработан проект Руководства по представлению документов первого модуля регистрационного досье лекарственного препарата в форме электронного общего технического документа в государства признания.
Такое решение принято Распоряжением Совета ЕЭК от 17 октября 2022 года № 34. Проработка вопроса о целесообразности внесения изменений в Правила регистрации и экспертизы лекарственных средств для медицинского применения, утвержденные Решением Совета ЕЭК от 3 ноября 2016 года № 78, в части признания по инициативе уполномоченного органа результатов регистрации лекарственных средств для медицинского применения, зарегистрированных в государствах-членах ЕАЭС, будет проводиться Коллегией ЕЭК совместно с заинтересованными уполномоченными органами.
Совет Евразийской экономической комиссии утвердил план мероприятий (дорожную карту) по переходу на регистрацию медицинских изделий согласно праву Союза. Об этом сообщает Отдел информационного обеспечения Департамента протокола и организационного обеспечения ЕЭК.
Департаментом технического регулирования и аккредитации ЕЭК разработан перечень действующих веществ и нерациональных комбинаций действующих веществ, медицинское применение которых в качестве лекарственных препаратов признано нерациональным.
Департаментом технического регулирования и аккредитации ЕЭК разработан проект документа с новыми изменениями в Правила проведения исследований биологических лекарственных средств ЕАЭС. В настоящее время он размещен на правовом портале ЕЭК для общественного обсуждения, которое завершится 18 декабря 2022 года.
Коллегией ЕЭК разработан проект руководства по обеспечению целостности данных и валидации компьютеризированных систем. Проект опубликован на правовом портале ЕАЭС. Его общественное обсуждение продлится до 15 декабря 2022 года.
Об этом сообщил министр по техническому регулированию ЕЭК Виктор Назаренко на 2-м Всероссийском форуме с международным участием «NOVAMED-2022», который проходил в Москве с 10 по 11 ноября 2022 года.
На правовом портале Евразийской экономической комиссии опубликовано Решение Совет ЕЭК от 17 октября 2022 года № 160, которым предусмотрено проведение таможенных операций в первоочередном порядке для ряда товаров, подвергающихся быстрой порче.
- В ЕАЭС разработана концепция сбора и использования данных реальной клинической практики
- Одобрена вторая часть Фармакопеи ЕАЭС. Изменения вступают в силу с 1 апреля 2023 года
- ЕЭК продлила ставки нулевых пошлин на полимерную пленку для медицинских изделий
- В ЕАЭС утверждено руководство по составлению нормативного документа по качеству ЛС