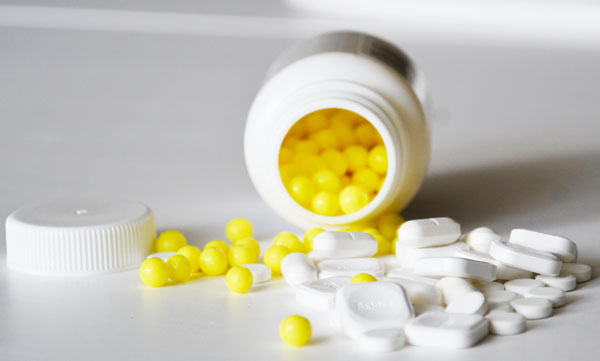
Совет Евразийской экономической комиссии (ЕЭК) принял решение продлить срок освобождения от ввозной таможенной пошлины ряда товаров, используемых для предупреждения и предотвращения распространения коронавирусной инфекции. Тарифная льгота продлевается с 1 октября по 31 марта 2021 года.
Все материалы
Вопросы предотвращения распространения COVID-19, контроля за безопасностью пищевой продукции на потребительском рынке, регулирования обращения лекарственных средств и медицинских изделий, а также Фармакопею Евразийского экономического союза и цели устойчивого развития обсудили член Коллегии (министр) по техническому регулированию Евразийской экономической комиссии Виктор Назаренко и директор Европейского регионального бюро Всемирной организации здравоохранении Ханс Клюге в штаб-квартире ЕЭК.
На официальном правовом портале Евразийского экономического союза docs.eaeunion.org 18 сентября опубликована Рекомендация Коллегии ЕЭК №15 «О руководствах по оценке качества и исследованию биоэквивалентности отдельных групп лекарственных препаратов», принятая 15 сентября 2020 года.
15 сентября 2020 года Решением Коллегии Евразийской экономической комиссии №111 утверждено Руководство по фармакокинетическому и клиническому изучению биоэквивалентности липосомальных лекарственных препаратов (ЛП) для внутривенного введения. Документ опубликован на правовом портале ЕАЭС docs.eaeunion.org 18 сентября 2020 года и вступает в силу по истечении 6 месяцев с даты его официального опубликования.
Коллегия Евразийской экономической комиссии приняла два руководства, регламентирующие процесс фармацевтической разработки и подтверждения эквивалентной эффективности и безопасности мицеллярных и нанопрепаратов.
Экспертный комитет по лекарственным средствам Евразийской экономической комиссии под председательством члена Коллегии (министра) по техническому регулированию ЕЭК Виктора Назаренко одобрил проекты документов, обеспечивающие применение государствами-членами единых подходов к обращению лекарств на общем рынке Евразийского экономического союза.
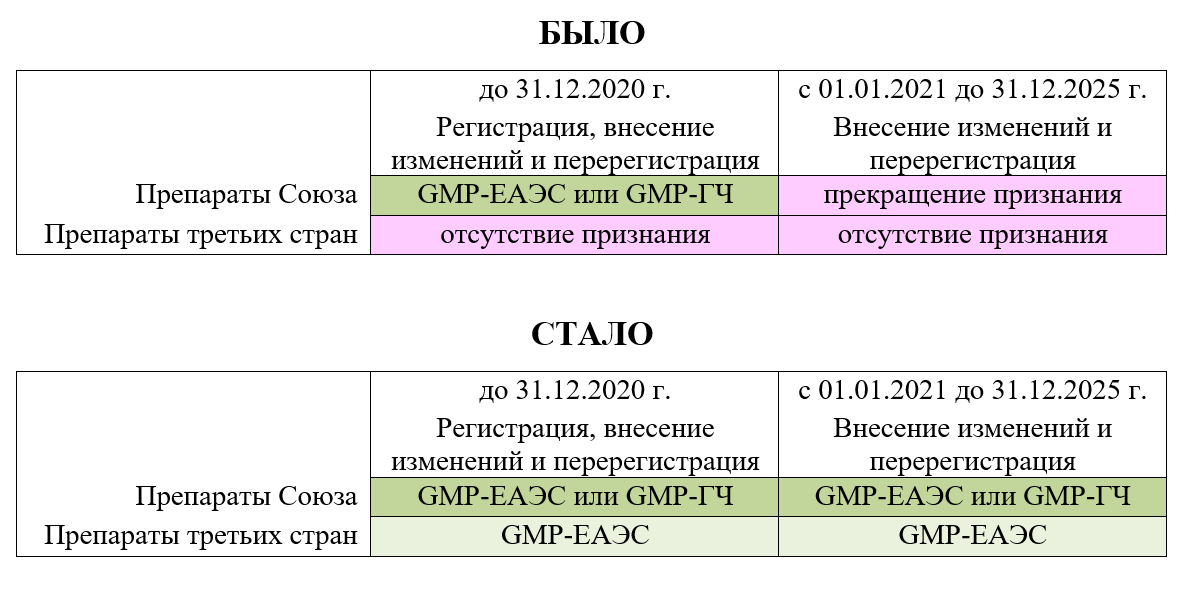
Совет Евразийской экономической комиссии 4 сентября расширил положения Решения Совета Комиссии от 3 ноября 2016 г. №93 «О признании результатов инспектирования производства лекарственных средств» в части взаимного признания при национальной регистрации сертификатов GMP Союза за счет их применения для лекарственных препаратов, произведенных за пределами Евразийского экономического союза.
Совет Евразийской экономической комиссии (ЕЭК) 4 сентября 2020 года утвердил изменения в правила проведения исследований биоэквивалентности лекарственных препаратов. Они дополнены двумя новыми приложениями, которые позволят установить единые подходы для подтверждения равной эффективности и взаимозаменяемости таких групп лекарственных препаратов, как мази, гели и кремы для местного применения, а также таблеток и капсул продленного отсроченного действия.
Коллегией ЕЭК разработан проект Руководства по трансферу технологий и аналитических методик при производстве лекарственных средств в целях гармонизации требований к производству лекарств, установленных законодательством государств-членов ЕАЭС.
Решением Коллегии ЕЭК утверждена Фармакопея Евразийского экономического союза. Документом установлено, что до 1 января 2026 г. регистрационные досье лекарственных средств для медицинского применения и ветеринарных лекарственных средств должны быть приведены в соответствие с требованиями утвержденной Фармакопеи Евразийского экономического союза.
Своим распоряжением №16 от 17 яюля 2020 года Евразийский межправительственный совет утвердил Комплексный план мероприятий в области здравоохранения и санитарно-эпидемиологического благополучия населения по предотвращению распространения коронавирусной инфекции COVID-19 и иных инфекционных заболеваний на территориях государств-членов Евразийского экономического союза.
Советом Евразийской экономической комиссии разработан проект решения о внесении изменений в технический регламент Таможенного союза «О безопасности пищевой продукции» (ТР ТС 021/2011), а также в технический регламент Таможенного союза «О безопасности отдельных видов специализированной пищевой продукции, в том числе диетического лечебного и диетического профилактического питания» (ТР ТС 027/2012). Изменения в технические регламенты вносятся с целью установления специальных требований к биологически активным добавкам к пище (далее - БАД). Для реализации этой цели специальные требования к БАД исключаются из ТР ТС 021/2011, а в ТР ТС 027/2012 вносятся изменения, касающиеся их производства, реализации и маркировки.
Коллегия Евразийской экономической комиссии утвердила Фармакопею ЕАЭС, которая станет основой единого подхода к оценке качества лекарственных средств для пяти союзных стран, сообщается на сайте ЕЭК. Документ начнет действовать с 1 марта 2021 года. Производителям лекарственных препаратов, ранее зарегистрированных на общем рынке Союза, предоставлен 5-летний срок – до 1 января 2026 года – для приведения своих нормативных документов по качеству лекарственных средств в соответствие с Фармакопеей Союза.